Mua thuốc Tamiflu 75mg chính hãng ở đâu? Bán giá bao nhiêu? Hà Nội
Liên hệ để biết giá !
Nội dung mô tả tóm tắt: Thuốc Tamiflu 75mg mua ở đâu? thuốc Tamiflu giá bao nhiêu? địa chỉ bán thuốc Tamiflu. công dụng, cách dùng thuốc Tamiflu LH Ds Dũng để được tư vấn.
Chỉ định
Tamiflu được chỉ định để điều trị bệnh cúm ở người lớn và trẻ em từ một tuổi trở lên.
Tamiflu được chỉ định để phòng ngừa bệnh cúm ở người lớn và trẻ em từ một tuổi trở lên.
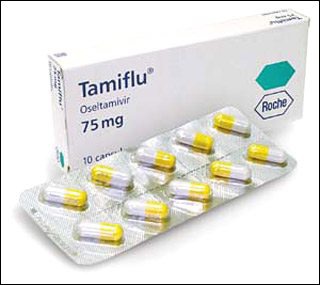
TAMIFLU 75MG LÀ THUỐC GÌ?
Thuốc Tamiflu chứa thành phần Oseltamivir; 30mg, 45mg hoặc 75mg, do công ty Dược phẩm Hoffmann – La Roche sản xuất. Thuốc được chỉ định trong phòng và điều trị ở người lớn và trẻ em trên 1 tuổi.
Quy cách
Viên nang 30 mg : hộp 1 vỉ x 10 viên,
Viên nang 45 mg : hộp 1 vỉ x 10 viên,
Viên nang 75 mg : hộp 1 vỉ x 10 viên,
Bột pha huyền dịch uống : hộp 1 lọ
MUA THUỐC TAMIFLU Ở ĐÂU? BÁN GIÁ BAO NHIÊU?
Thuốc Tamiflu phòng và điều trị cúm ở người lớn và trẻ em trên 1 tuổi có bán tại hệ thông Thuockedon24h.com, chúng tôi cam kết hàng chính hãng, chất lượng tốt và giá cả hợp lý nhất.
Giá thuốc Tamiflu 75mg khoảng 90-100k/viên, hộp 10 viên.
LIỀU LƯỢNG VÀ CÁCH DÙNG THUỐC TAMIFLU 75MG
Tamiflu có thể được dùng kèm hoặc không kèm theo thức ăn. (Xem mục Dược động học). Tuy nhiên, dùng Tamiflu kèm với thức ăn có thể làm tăng khả năng dung nạp thuốc ở một số bệnh nhân.
Trong trường hợp hỗn dịch uống Tamiflu không sẵn có, người lớn, thanh thiếu niên và trẻ em không thể nuốt viên thuốc, có thể uống Tamiflu bằng cách mở viên nang và cho toàn bộ lượng thuốc trong viên nang vào một lượng vừa đủ (tối đa 1 thìa cà phê) thức uống ngọt như siro chocolate thường hoặc loại không đường, mật ong (chỉ dành cho trẻ em trên hai tuổi), đường nâu sáng hoặc đường tinh khiết hoà tan trong nước, kem tươi, sữa đặc có đường, nước sốt táo hoặc sữa chua để che giấu vị đắng của thuốc. Khuấy đều hỗn hợp và đưa cho bệnh nhân. Cần uống hỗn hợp này ngay sau khi pha chế.
Liều chuẩn:
Điều trị bệnh cúm
Nên bắt đầu điều trị vào ngày thứ nhất hoặc ngày thứ hai khi xuất hiện các triệu chứng đầu tiên của bệnh cúm
Người lớn và thanh thiếu niên:
Ở người lớn và thiếu niên từ 13 tuổi trở lên, liều khuyên dùng là uống viên nang Tamiflu 75mg hai lần mỗi ngày, trong 5 ngày. Trong trường hợp không thể nuốt được viên nang, có thể dùng dạng huyền dịch với liều 75mg Tamiflu hai lần mỗi ngày, trong 5 ngày.
Trẻ em:
Trẻ có cân nặng trên 40kg nếu có thể nuốt được viên nang, cũng sẽ được điều trị với liều uống viên nang 75mg hai lần mỗi ngày, thay vì dùng Tamiflu dạng huyền dịch với liều khuyên dùng như bảng dưới đây:
Liều uống được khuyên dùng của Tamiflu cho trẻ từ một tuổi trở lên:
Trọng lượng cơ thể Liều khuyên dùng trong 5 ngày
≤ 15kg 30 mg hai lần mỗi ngày
> 15kg đến 23kg 45 mg hai lần mỗi ngày
> 23kg đến 40kg 60 mg hai lần mỗi ngày
> 40kg 75 mg hai lần mỗi ngày
Có sẵn bơm định liều được đánh dấu các mức liều dùng 30mg, 45mg và 60mg cho dạng huyền dịch uống
Tamiflu dạng bột pha huyền dịch uống nên được pha chế bởi dược sĩ trước khi dùng cho bệnh nhân (Xem mục Hướng dẫn đặc biệt cho việc sử dụng và tiêu hủy thuốc)
Phòng ngừa bệnh cúm
Người lớn và thanh thiếu niên:
Liều khuyên dùng để phòng ngừa bệnh cúm là sau khi tiếp xúc với người bị nhiễm cúm, nên uống Tamiflu 75mg ngày một lần, trong 10 ngày. Nên bắt đầu việc điều trị trong vòng hai ngày sau khi tiếp xúc với nguồn bệnh. Liều khuyên dùng để phòng bệnh cúm trong suốt thời gian có dịch ở cộng đồng là dùng 75mg ngày một lần. Tính an toàn và hiệu quả của việc dùng thuốc đã được chứng minh cho tới 6 tuần. Chừng nào vẫn còn dùng thuốc thì thời gian bảo vệ của thuốc vẫn còn.
Trẻ em:
Trẻ có cân nặng trên 40kg nếu có thể nuốt được viên nang, sẽ được điều trị phòng bệnh cúm với viên nang 75mg, uống ngày một lần, trong 10 ngày, thay vì dùng Tamiflu dạng huyền dịch với liều khuyên dùng như bảng dưới đây:
Liều uống được khuyên dùng của Tamiflu để phòng ngừa bệnh cúm cho trẻ từ một tuổi trở lên:
Trọng lượng cơ thể Liều khuyên dùng trong 10 ngày
≤ 15kg 30 mg ngày một lần
> 15kg đến 23kg 45 mg ngày một lần
> 23kg đến 40kg 60 mg ngày một lần
> 40kg 75 mg ngày một lần
Có sẵn bơm định liều đánh dấu các mức liều dùng 30mg, 45mg và 60mg cho dạng huyền dịch uống
Tamiflu dạng bột pha huyền dịch uống nên được pha chế bởi dược sĩ trước khi dùng cho bệnh nhân
MỘT SỐ THÔNG TIN KHÁC CỦA TAMIFLU
Dược lực
Cơ chế tác dụng
Oseltamivir phosphate là tiền chất của oseltamivir carboxylate (OC), một chất ức chế chọn lọc và có hiệu quả men neuraminidase của virus cúm A và B. Men này có vai trò quan trọng trong việc vừa giúp virus xâm nhập vào những tế bào lành, vừa giúp cho việc giải phóng các phần virus mới được tạo thành từ các tế bào bị nhiễm, và do đó làm lan nhanh quá trình nhiễm virus.
Oseltamivir carboxylate ức chế men neuraminidase của virus cúm cả 2 type A và B. Nồng độ OC cần thiết để ức chế 50% hoạt tính men (IC50) ở giới hạn nanomol thấp. OC vừa ức chế sự lây nhiễm và sao chép của virus cúm in-vitro, vừa ức chế sự sao chép và gây bệnh của virus cúm in-vivo.
OC làm giảm sự lan tràn của virus cúm cả type A lẫn type B bằng cách ức chế việc giải phóng các virus gây nhiễm ra khỏi tế bào bị nhiễm.
Các nghiên cứu về hiệu quả trên lâm sàng
Hiệu quả lâm sàng của Tamiflu đã được chứng minh qua các nghiên cứu nhiễm virus thực nghiệm ở người và qua các nghiên cứu pha III của quá trình nhiễm tự nhiên virus cúm.
Trong các nghiên cứu trên thì việc điều trị bằng Tamiflu không ảnh hưởng đến sự đáp ứng kháng thể dịch thể chống lại quá trình nhiễm. Đáp ứng sinh kháng thể với vaccine bất hoạt khó có thể bị ảnh hưởng khi dùng Tamiflu.
Các thử nghiệm ở các trường hợp mắc cúm tự nhiên
Trong các thử nghiệm lâm sàng pha III, được tiến hành vào mùa cúm Bắc Bán cầu năm 1997-1998, những bệnh nhân được điều trị Tamiflu trong vòng 40 giờ sau khi có các triệu chứng đầu tiên. Trong những nghiên cứu này, 97% bệnh nhân bị nhiễm virus cúm A và 3% nhiễm virus cúm B. Điều trị với Tamiflu làm giảm đáng kể thời gian biểu hiện lâm sàng các dấu hiệu và triệu chứng của cúm tới 32 giờ. Mức độ nặng của bệnh cũng giảm khoảng 38% ở nhóm những bệnh nhân bị cúm được điều trị với Tamiflu, khi so sánh với nhóm dùng giả dược. Hơn nữa, Tamiflu làm giảm tỉ lệ biến chứng do điều trị cúm bằng liệu pháp kháng sinh ở những người trẻ, khỏe mạnh xấp xỉ 50%. Những biến chứng này gồm viêm phế quản, viêm phổi, viêm xoang và viêm tai giữa. Các thử nghiệm lâm sàng pha III này cho thấy những bằng chứng rõ rệt về các tác dụng thứ phát lên hoạt tính kháng virus ở cả việc giảm thời gian lan tràn của virus và cả việc giảm AUC của lượng virus.
Các dữ liệu thu được từ một nghiên cứu điều trị ở đối tượng người lớn tuổi cho thấy dùng Tamiflu 75mg, 2 lần mỗi ngày, trong 5 ngày có thể làm giảm thời gian trung vị của bệnh về mặt lâm sàng, tương tự như kết quả thu được từ nghiên cứu điều trị ở những người trẻ tuổi. Trong một nghiên cứu riêng biệt, những bệnh nhân trên 13 tuổi bị cúm có kèm theo bệnh tim và/hoặc bệnh phổi mãn tính đã được điều trị cùng một chế độ hoặc là Tamiflu, hoặc là giả dược. Không có sự khác biệt về thời gian trung vị đến khi giảm toàn bộ các triệu chứng được ghi nhận giữa nhóm dùng Tamiflu và nhóm dùng giả dược, tuy nhiên, thời gian bị sốt giảm xuống khoảng một ngày ở nhóm dùng Tamiflu. Tỷ lệ bệnh nhân có virus phát tán ở ngày thứ 2 và thứ 4 cũng giảm đáng kể nếu được điều trị tích cực. Về mặt an toàn thì không có sự khác nhau giữa những đối tượng có nguy cơ cao và nhóm đối tượng bình thường
Điều trị bệnh cúm ở trẻ em
Một thử nghiệm điều trị mù đôi có kiểm chứng với giả dược đã được tiến hành ở trẻ em, từ 1 đến 12 tuổi (tuổi trung bình là 5,3). Những bé này có sốt (> 1000F/37,8oC) cộng với một triệu chứng về hô hấp (ho hoặc sổ mũi), với sự hiện diện của virus cúm trong cộng đồng. Trong nghiên cứu này, 67% bệnh nhi nhiễm virus cúm typ A và 33% nhiễm virus cúm typ B. Điều trị bằng Tamiflu, bắt đầu trong vòng 48 giờ khi có triệu chứng đầu tiên, đã làm giảm đáng kể thời gian bệnh khoảng 35,8 giờ so với giả dược. Thời gian bệnh được xác định là thời gian giảm các triệu chứng ho, sung huyết mũi, giảm sốt và trở về tình trạng sức khoẻ và hoạt động bình thường. Tỷ lệ bệnh nhân bị viêm tai giữa cấp giảm khoảng 40% ở những bé được điều trị bằng Tamiflu so với dùng giả dược. Những bé được điều trị bằng Tamiflu cũng trở về tình trạng sức khỏe và hoạt động bình thường sớm hơn khoảng hai ngày so với những bé được dùng giả dược.
Một nghiên cứu thứ hai đã hoàn tất ở 334 bé bị hen phế quản từ 6 đến 12 tuổi, trong đó 53,6% có virus cúm dương tính. Ở nhóm được điều trị bằng oseltamivir, thời gian bệnh trung bình không được giảm đáng kể. Vào ngày thứ 6 (ngày điều trị cuối cùng), FEV1 tăng khoảng 10,8% ở nhóm được điều trị bằng oseltamivir, trong khi ở nhóm dùng giả dược (p=0,0148), chỉ tăng 4,7%.
Các thử nghiệm phòng bệnh cúm
Phòng bệnh cúm ở người trưởng thành và thanh thiếu niên
Tính hiệu quả của Tamiflu trong việc phòng bệnh cúm A và B mắc phải tự nhiên, đã được chứng minh trong ba nghiên cứu phase III riêng biệt.
Trong một thử nghiệm phase III ở người trưởng thành và thanh thiếu niên tiếp xúc với người bị cúm sống trong cùng một nhà, Tamiflu được bắt đầu dùng trong vòng 2 ngày từ khi những đối tượng này có triệu chứng cúm đầu tiên và dùng liên tục trong 7 ngày, đã làm giảm đáng kể tỷ lệ mắc cúm do tiếp xúc khoảng 92%.
Trong một nghiên cứu mù đôi, có đối chứng với giả dược được tiến hành ở những người trưởng thành khỏe mạnh chưa được tiêm chủng, tuổi từ 18-65, Tamiflu làm giảm đáng kể tỷ lệ bệnh cúm trên lâm sàng khoảng 76%, trong suốt thời gian có dịch cúm tại cộng đồng. Những đối tượng trong nghiên cứu này đã dùng Tamiflu trong 42 ngày. Trong một nghiên cứu mù đôi, có đối chứng với giả dược ở những người già sống trong nhà dưỡng lão, 80% trong số họ được tiêm chủng vào mùa cúm khi nghiên cứu này được tiến hành, Tamiflu làm giảm đáng kể tỷ lệ bệnh cúm trên lâm sàng khoảng 92%. Cũng trong nghiên cứu này, Tamiflu làm giảm đáng kể tỷ lệ viêm phế quản, viêm phổi và viêm xoang có liên quan đến bệnh cúm khoảng 86%. Những đối tượng trong nghiên cứu này đã dùng Tamiflu trong 42 ngày.
Trong cả ba thử nghiệm lâm sàng trên, khoảng 1% số đối tượng dùng Tamiflu để phòng cúm phát triển trong suốt quá trình dùng thuốc.
Trong các thử nghiệm lâm sàng phase III này, Tamiflu cũng làm giảm đáng kể tỷ lệ phát tán virus và ngăn chặn sự lan truyền virus trong gia đình một cách thành công.
Phòng bệnh cúm ở trẻ em
Tính hiệu quả của Tamiflu trong việc ngăn ngừa bệnh cúm mắc phải tự nhiên đã được chứng minh trong một nghiên cứu phòng bệnh cúm sau khi tiếp xúc với nguồn nhiễm. Nghiên cứu này được tiến hành tại nhà và gồm những bé từ 1 đến 12 tuổi, cả những trường hợp đã được chỉ rõ lẫn những trường hợp tiếp xúc trong gia đình. Thông số chính để đánh giá tính hiệu quả của thuốc trong nghiên cứu này là tỷ lệ mắc bệnh cúm trên lâm sàng có kết quả xét nghiệm dương tính với virus. Trong nghiên cứu này, Tamiflu dạng huyền dịch uống với liều từ 30mg đến 75mg, mỗi ngày một lần, trong 10 ngày đã được dùng cho những bé chưa bị phát tán virus quá ngưỡng, cho thấy đã làm giảm tỷ lệ mắc bệnh cúm trên lâm sàng có kết quả xét nghiệm dương tính với virus từ 21% (15/70) ở nhóm trẻ không được điều trị dự phòng so với 4% (2/47) ở nhóm trẻ được điều trị dự phòng.
Sự đề kháng của virus
Các nghiên cứu lâm sàng được tiến hành cho đến nay trong việc phòng bệnh cúm sau tiếp xúc (7 ngày), sau tiếp xúc trong gia đình (10 ngày) và phòng bệnh cúm theo mùa (42 ngày) không cho thấy có bằng chứng nào về sự kháng thuốc liên quan đến việc sử dụng Tamiflu.
Nguy cơ xuất hiện kháng thuốc khi sử dụng trên lâm sàng để điều trị cúm đã được nghiên cứu kỹ. Trong tất cả các nghiên cứu lâm sàng do Roche tài trợ về các trường hợp nhiễm bệnh tự nhiên, bất chấp liều điều trị, tỷ lệ bệnh nhân được phát hiện mang virus cúm đề kháng với oseltamivir ở người lớn và trẻ vị thành niên là 0,32% (4/1245) xác định bởi kiểu hình và 0,4% (5/1245) xác định bởi kiểu hình và kiểu gen (xác định hoàn toàn bởi kiểu gen không được thực hiện ở tất cả các nghiên cứu), và lần lượt là 4,1% (19/464) và 5,4% (25/464) ở trẻ em từ 1 -12. Tất cả các bệnh nhân này được phát hiện chỉ mang virus đề kháng với oseltamivir carboxylate thoáng qua. Những bệnh nhân mang virus kháng thuốc này vẫn thải trừ được virus như thường lệ và không diễn tiến xấu về mặt lâm sàng.
Nhiều dạng đột biến kháng thuốc khác nhau ở men neuraminidase của virus được chọn lọc trong phòng thí nghiệm trong các nghiên cứu của Roche hoặc được đăng tải trên các y văn. Đột biến kháng thuốc có khuynh hướng chuyên biệt theo từng kiểu phụ của virus. Mức độ giảm tính nhạy cảm thay đổi rõ rệt đối với các đột biến khác nhau từ 2 lần đối với 1222V ở N1 đến 30.000 lần đối với R292K ở N2. Đối với virus cúm B đột biến kháng thuốc ở men neuraminidase không được chọn lọc trong phòng thí nghiệm. Trong các nghiên cứu lâm sàng và virus có được từ bệnh nhân được điều trị với Tamiflu, đột biến ở men neuraminidase N1 (bao gồm cả virus H5N1) gây đề kháng/giảm độ nhạy cảm với oseltamivir carboxylate là H274Y và một trường hợp là N294S) và E119V, R292K và một trường hợp là N294S và SASG254-248del ở men neuraminidase N2. Ở men neuraminidase của virus cúm B có một trường hợp G402S giảm độ nhạy cảm xuống 4 lần được báo cáo và một trường hợp D198N (giảm 10 lần) ở trẻ suy giảm miễn dịch cũng được báo cáo. Những virus có kiểu gen neuraminidase đề kháng có độ mất tương thích thay đổi so với chủng phân lập tự nhiên. Những nghiên cứu ở chuột và chồn về tính nhiễm khuẩn, sinh bệnh và lây truyền chỉ ra rằng R292K ở N2 yếu thế hơn nhiều so với E119V ở N2 và D198N ở B cho thấy ít thay đổi so với chủng phân lập tự nhiên. H274Y ở N1 và N294S ở N2 thì ở mức độ trung bình.
Dược động học
Hấp thu
Oseltamivir được hấp thu nhanh chóng ở đường tiêu hóa sau khi uống oseltamivir phosphate và một phần lớn thuốc được chuyển hóa thành chất có hoạt tính, chủ yếu nhờ men esterase ở gan. Nồng độ trong huyết tương của chất chuyển hóa có hoạt tính có thể tính được trong vòng 30 phút, đạt mức gần cực đại sau khi dùng thuốc 2-3 giờ và vượt đáng kể (> 20 lần) nồng độ của thuốc ban đầu. Có ít nhất 75% lượng thuốc uống vào được tuần hoàn dưới dạng chất chuyển hóa có hoạt tính. Nồng độ trong huyết tương của chất chuyển hóa có hoạt tính tỷ lệ với liều dùng và không bị ảnh hưởng bởi thức ăn dùng cùng (Xem mục Liều lượng và Cách dùng)
Phân bố
Thể tích phân bố trung bình (Vss) của chất chuyển hóa có hoạt tính là khoảng 23 lít ở người. Gốc có hoạt tính tới được tất cả các vị trí quan trọng bị nhiễm virus cúm qua nghiên cứu trên chồn, chuột và thỏ. Trong những nghiên cứu này, người ta đã thấy nồng độ kháng virus của chất chuyển hóa có hoạt tính tập trung ở phổi, dịch rửa phế quản-phế nang, chất nhầy ở mũi, tai giữa và khí quản sau khi uống oseltamivir phosphate.
Mức độ gắn kết của chất chuyển hóa có hoạt tính với protein huyết tương ở người là không đáng kể (xấp xỉ 3%). Mức gắn vào protein huyết tương ở người của tiền dược là 42%. Với mức này thì chưa đủ để gây ra các tương tác thuốc có ý nghĩa.
Chuyển hóa
Một lượng lớn oseltamivir phosphate được chuyển hóa thành chất chuyển hóa có hoạt tính nhờ men esterase, men này khu trú chủ yếu ở gan. Cả oseltamivir lẫn chất chuyển hóa có hoạt tính đều không phải là cơ chất hoặc chất ức chế của các cytochrome P450 isoforms (Xem mục Tương tác thuốc)
Thải trừ
Oseltamivir sau khi hấp thu được thải trừ phần lớn (> 90%) bằng cách chuyển thành chất chuyển hóa có hoạt tính. Chất này không bị chuyển hóa tiếp mà bị thải trừ qua nước tiểu. Nồng độ đỉnh của chất chuyển hóa có hoạt tính trong huyết tương giảm dần với thời gian bán thải từ 6 đến 10 giờ trong đa số trường hợp.
Thuốc có hoạt tính được thải trừ toàn bộ (> 99%) qua thận. Độ thanh thải thận (18,8 lít/giờ) vượt quá mức lọc cầu thận (7,5 lít/giờ) cho thấy thuốc còn được thải trừ tiếp qua ống thận. Dưới 20% liều uống có đánh dấu phóng xạ được thải trừ qua phân.
Dược động học ở nhóm bệnh nhân đặc biệt
Bệnh nhân suy thận
Sau khi dùng 100mg Tamiflu, 2 lần/ngày, trong thời gian 5 ngày cho những bênh nhân bị suy thận ở các mức độ khác nhau, người ta thấy nồng độ chất chuyển hóa có hoạt tính tỷ lệ nghịch với sự suy giảm chức năng thận.
Điều trị bệnh cúm
Không cần điều chỉnh liều cho những bệnh nhân có độ thanh thải creatinine trên 30 ml/phút. Ở những bệnh nhân có độ thanh thải creatinine từ 10-30 ml/phút, cần giảm liều Tamiflu xuống 75mg uống ngày một lần, trong 5 ngày. Không có liều khuyên dùng cho những bệnh nhân bị bệnh thận giai đoạn cuối đang được lọc máu thường qui và thẩm phân phúc mạc liên tục, cũng như những bệnh nhân có độ thanh thải creatinine ≤ 10 ml/phút (Xem mục Các hướng dẫn liều dùng đặc biệt và mục Chú ý đề phòng và Thận trọng lúc dùng)
Phòng ngừa bệnh cúm
Ở những bệnh nhân có độ thanh thải creatinine từ 10-30 ml/phút, liều dùng nên được giảm xuống còn 75mg Tamiflu, cách một ngày uống một lần, hoặc uống 30mg dạng huyền dịch mỗi ngày. Không có liều khuyên dùng cho những bệnh nhân bị bệnh thận giai đoạn cuối đang được lọc máu thường qui và thẩm phân phúc mạc liên tục, cũng như những bệnh nhân có độ thanh thải creatinine ≤ 10 ml/phút (Xem mục Các hướng dẫn liều dùng đặc biệt và mục Chú ý đề phòng và Thận trọng lúc dùng)
Bệnh nhân suy gan
Dựa trên những nghiên cứu trong phòng thí nghiệm và trên động vật, ở những bệnh nhân suy gan nhẹ hoặc trung bình, gia tăng đáng kể nồng độ oseltamivir và chất chuyển hóa có hoạt tính không được ghi nhận và điều này đã được xác định lại trong các nghiên cứu lâm sàng (Xem mục Hướng dẫn liều dùng đặc biệt). Độ an toàn và đặc tính dược động học ở bệnh nhân suy gan nặng chưa được nghiên cứu.
Người già
Ở người lớn tuổi (từ 65 đến 78 tuổi), nồng độ của chất chuyển hóa có hoạt tính ở trạng thái ổn định cao hơn khoảng 25-35% so với người trẻ khi dùng cùng một liều Tamiflu. Thời gian bán thải của thuốc ở người già tương tự như ở người trẻ. Căn cứ vào nồng độ của thuốc và khả năng dung nạp, không cần điều chỉnh liều cho người già khi được điều trị hoặc phòng ngừa bệnh cúm (Xem mục Các hướng dẫn liều dùng đặc biệt)
Trẻ em
Dược động học của Tamiflu đã được đánh giá trong một nghiên cứu dược động học liều đơn ở trẻ em từ 1 đến 16 tuổi. Dược động học đa liều cũng đã được nghiên cứu ở một số ít trẻ từ 3 đến 12 tuổi trong một thử nghiệm lâm sàng. Trẻ nhỏ tuổi có mức độ thải trừ tiền dược và chất chuyển hóa có hoạt tính nhanh hơn so với trẻ lớn tuổi, làm cho nồng độ thuốc trở nên thấp hơn nếu xét theo liều được cho tính bằng mg/kg. Liều 2mg/kg cho nồng độ tác dụng của oseltamivir carboxylate tương tự với nồng độ đạt được ở người lớn dùng liều đơn viên nang 75mg (xấp xỉ 1mg/kg). Dược động học của oseltamivir ở trẻ em trên 12 tuổi tương tự như ở người lớn.
An toàn tiền lâm sàng
Những dữ liệu tiền lâm sàng không cho thấy mối nguy hiểm đặc biệt nào của thuốc cho người dựa trên các nghiên cứu thông thường về dược học an toàn, độc tính liều lặp lại và sự nhiễm độc gen.
Tính sinh ung thư
Ba nghiên cứu về khả năng gây ung thư (các nghiên cứu hai năm ở chuột nhắt và chuột lớn với oseltamivir, và thử nghiệm sáu tháng về trao đổi gen Tg: AC ở chuột nhắt được tiến hành với chất chuyển hóa có hoạt tính) cho kết quả âm tính.
Tính gây đột biến
Oseltamivir và chất chuyển hóa có hoạt tính cho kết quả âm tính trong lô thử nghiệm chuẩn gây độc trên gen
Suy giảm khả năng sinh sản
Nghiên cứu về khả năng sinh sản ở chuột với liều lên tới 1500mg/kg/ngày đã chứng minh không có tác động có hại nào lên cả hai giới.
Các nghiên cứu về quái thai đã được tiến hành với liều lên tới 1500mg/kg/ngày ở chuột và 500mg/kg/ngày ở thỏ. Không ghi nhận được tác động nào của thuốc lên sự phát triển của phôi thai. Trong các nghiên cứu chu sinh ở chuột, quá trình chuyển dạ kéo dài được ghi nhận ở liều 1500mg/kg/ngày: giới hạn an toàn giữa liều điều trị ở người và liều cao nhất không gây hại (500mg/kg/ngày) ở chuột là gấp 480 lần đối với oseltamivir và gấp 44 lần đối với chất chuyển hóa có hoạt tính. Nồng độ thuốc ở phôi chuột và phôi thỏ xấp xỉ 15 đến 20% nồng độ ở mẹ.
Đặc tính khác
Ở chuột cho con bú, oseltamivir và chất chuyển hoá có hoạt tính được bài tiết vào trong sữa. Ở người, vẫn chưa biết liệu oseltamivir và chất chuyển hoá có hoạt tính có được bài tiết vào trong sữa mẹ hay không, thế nhưng từ phép ngoại suy các dữ liệu ở động vật, có thể dự đoán có khoảng 0,01mg oseltamivir và 0,3mg chất chuyển hóa có hoạt tính được bài tiết vào trong sữa mẹ mỗi ngày.
Khả năng da nhạy cảm với oseltamivir được ghi nhận trong một xét nghiệm "tối đa hóa" ở chuột lang. Sau khi gây kích ứng với dị nguyên những con vật thí nghiệm này, người ta thấy có khoảng 50% con vật được điều trị với hoạt chất chính đơn thuần có xuất hiện ban đỏ. Sự gây kích ứng có hồi phục ở mắt thỏ cũng đã được phát hiện.
Trong khi liều rất cao oseltamivir phosphat dùng đường uống không gây ra một biến cố bất lợi nào ở chuột trưởng thành, thì liều này lại gây độc tính ở chuột con 7 ngày tuổi, kể cả tử vong. Những biến cố bất lợi này đã được ghi nhận với liều 657 mg/kg và cao hơn. Ở liều 500 mg/kg, không có biến cố bất lợi nào được ghi nhận, kể cả khi điều trị lâu dài (chuột 7 đến 21 ngày tuổi dùng liều 500 mg/kg/ngày).
Chỉ định
Tamiflu được chỉ định để điều trị bệnh cúm ở người lớn và trẻ em từ một tuổi trở lên. (Xem mục Chú ý đề phòng và Thận trọng lúc dùng và mục An toàn tiền lâm sàng).
Tamiflu được chỉ định để phòng ngừa bệnh cúm ở người lớn và trẻ em từ một tuổi trở lên.
Chống chỉ định
Quá mẫn với oseltamivir phosphate hoặc với bất kỳ thành phần nào của thuốc.
Chú ý đề phòng và thận trọng lúc dùng
Tổng quát
Co giật và hiện tượng rối loạn chức năng thần kinh giống như mê sảng đã được ghi nhận ở những bệnh nhân cúm dùng Tamiflu, chủ yếu xảy ra ở trẻ em và thanh thiếu niên. Trong một vài trường hợp rất hiếm gặp, tình trạng mê sảng này có thể gây nên chấn thương do tai nạn. Vai trò của Tamiflu đối với các hiện tượng này hiện vẫn chưa rõ và đã có những ghi nhận ở bệnh nhân bị cúm mà không dùng Tamiflu (xem phần Sau khi lưu hành thuốc).
Bệnh nhân (đặc biệt trẻ em và thanh thiếu niên), cần được giám sát chặt chẽ các dấu hiệu hành vi bất thường. Không thấy bằng chứng về hiệu quả của Tamiflu trong bất kỳ bệnh nào gây bởi các tác nhân không phải vi rút cúm type A và B.
Nên điều chỉnh liều khi dùng thuốc để điều trị hoặc phòng ngừa bệnh cúm cho những bệnh nhân có độ thanh thải creatinine từ 10-30 ml/phút. Không có liều khuyên dùng cho những bệnh nhân bị bệnh thận giai đoạn cuối đang được lọc máu thường qui và thẩm phân phúc mạc liên tục, cũng như những bệnh nhân có độ thanh thải creatinine ≤ 10 ml/phút (Xem mục Những hướng dẫn liều dùng đặc biệt và mục Dược động học ở những đối tượng đặc biệt)
Một lọ Tamiflu 30g để pha huyền dịch uống có chứa 25,713g sorbitol. Một liều 45mg oseltamivir uống hai lần mỗi ngày sẽ đưa vào cơ thể 2,6g sorbitol. Với những bệnh nhân bị bất dung nạp fructose di truyền, liều nói trên vượt quá mức sorbitol tối đa được khuyên dùng hàng ngày. Không nên dùng Tamiflu cho trẻ dưới một tuổi (Xem mục An toàn tiền lâm sàng)
Tác động lên khả năng lái xe và vận hành máy móc
Không ảnh hưởng.
Sử dụng ở trẻ em
Xem mục Hướng dẫn liều dùng đặc biệt và Dược động học ở những đối tượng đặc biệt
Sử dụng ở người lớn tuổi
Xem mục Hướng dẫn liều dùng đặc biệt và Dược động học ở những đối tượng đặc biệt
Suy thận
Xem mục Hướng dẫn liều dùng đặc biệt và Dược động học ở những đối tượng đặc biệt
Suy gan
Xem mục Hướng dẫn liều dùng đặc biệt và Dược động học ở những đối tượng đặc biệt.
Lúc có thai và lúc nuôi con bú
Phụ nữ có thai
Nguy cơ thai kỳ nhóm B
Những nghiên cứu về tác động của thuốc lên sự sinh sản ở động vật, được tiến hành trên chuột và thỏ, không ghi nhận hiện tượng quái thai nào. Những nghiên cứu về khả năng sinh sản và độc tính sinh sản đã được tiến hành trên chuột. Không thấy có bằng chứng về ảnh hưởng của thuốc lên khả năng sinh sản ở tất cả các liều oseltamivir được nghiên cứu. Ở chuột và thỏ, người ta thấy mức tác động của thuốc lên phôi thai xấp xỉ 15-20% mức tác động của thuốc lên thú mẹ.
Hiện tại, vẫn chưa có đầy đủ các dữ liệu về phụ nữ có thai sử dụng thuốc để có thể đánh giá được nguy cơ gây dị dạng bào thai hoặc gây độc tính cho thai của oseltamivir phosphate. Do vậy, chỉ nên dùng Tamiflu cho phụ nữ có thai nếu lợi ích của việc dùng thuốc nhiều hơn so với những nguy cơ có thể xảy ra cho thai nhi.
Bà mẹ cho con bú
Ở chuột cho con bú, oseltamivir và chất chuyển hóa có hoạt tính được bài tiết vào trong sữa. Ở người, vẫn chưa biết liệu oseltamivir và chất chuyển hóa có hoạt tính có được bài tiết vào trong sữa mẹ hay không, thế nhưng ước tính dựa trên các dữ liệu ở động vật, có thể dự đoán có khoảng 0,01mg oseltamivir và 0,3mg chất chuyển hóa có hoạt tính được bài tiết vào trong sữa mẹ mỗi ngày. Vì vậy, chỉ nên dùng Tamiflu cho phụ nữ đang cho con bú nếu lợi ích của việc dùng thuốc nhiều hơn so với những nguy cơ có thể xảy ra cho trẻ đang bú mẹ.
Tương tác thuốc
Thông tin từ những nghiên cứu về dược lý và dược động học của oseltamivir phosphate cho thấy ít có khả năng xảy ra tương tác thuốc có ý nghĩa về mặt lâm sàng.
Một lượng lớn oseltamivir phosphate được chuyển hóa thành hợp chất có hoạt tính nhờ esterase khu trú chủ yếu ở gan. Tương tác thuốc do sự cạnh tranh gắn esterase vẫn chưa được báo cáo nhiều trong y văn. Do oseltamivir và chất chuyển hóa có hoạt tính đều gắn kết kém với protein huyết tương, khả năng tương tác do chiếm chỗ của thuốc khó có thể xảy ra.
Các nghiên cứu in vitro cho thấy cả oseltamivir phosphate lẫn chất chuyển hóa có hoạt tính đều không phải là chất nền tốt cho men oxidase có chức năng hỗn hợp P450 hoặc cho men glucuronyl transferases. (Xem mục Dược động học). Không có cơ sở nào về mặt cơ chế cho thấy có sự tương tác giữa thuốc và thuốc ngừa thai dùng đường uống.
Cimetidine, một chất ức chế không đặc hiệu của các đồng dạng cytochrome P450 và là chất cạnh tranh với những thuốc gốc bazơ hoặc thuốc cation hóa để bài tiết qua ống thận, không có ảnh hưởng gì lên nồng độ trong huyết tương của oseltamivir hoặc chất chuyển hóa có hoạt tính của nó.
Xét về mặt lâm sàng, các tương tác thuốc quan trọng có liên quan đến sự cạnh tranh để bài tiết qua ống thận khó có thể xảy ra do giới hạn an toàn đã được biết của hầu hết các thuốc, đặc điểm thải trừ của chất chuyển hoá có hoạt tính (lọc ở vi cầu thận và tiết ở ống thận dưới dạng anion) và khả năng thải trừ của những đường này. Dùng thuốc đồng thời với probenecid sẽ làm tăng nồng độ các chất chuyển hóa có hoạt tính lên gần gấp đôi do làm giảm sự tiết chủ động của chúng ở ống thận. Tuy vậy, nhờ giới hạn an toàn của chất chuyển hóa có hoạt tính rất rộng nên không cần thiết phải điều chỉnh liều khi dùng thuốc chung với probenecid.
Dùng thuốc đồng thời với amoxicillin không làm thay đổi nồng độ của cả hai loại thuốc trong huyết tương, điều này cho thấy rằng sự cạnh tranh để được bài tiết dưới dạng anion là rất yếu.
Dùng thuốc đồng thời với paracetamol không làm thay đổi nồng độ trong huyết tương của oseltamivir, chất chuyển hóa có hoạt tính của nó, hoặc paracetamol.
Không có tương tác thuốc về dược động học giữa oseltamivir hoặc chất chuyển hóa chính của nó được ghi nhận khi dùng chung oseltamivir với paracetamol, acid acetylsalicylic, cimetidine hoặc các thuốc kháng acid (magnesium và hydroxid nhôm và carbonate canxi)
Trong các nghiên cứu lâm sàng để điều trị và dự phòng phase III, người ta đã dùng Tamiflu chung với các thuốc thông dụng khác như thuốc ức chế men chuyển (enalapril, captopril), các thiazide lợi tiểu (bendrofluazide), kháng sinh (penicillin, cephalosporin, azithromycin, erythromycin và doxycycline), thuốc chẹn thụ thể H2 (ranitidine, cimetidine), chẹn beta (propanolol), các xanthine (theophyline), thuốc giống giao cảm (pseudoephedrine), chế phẩm thuốc phiện (codeine), corticosteroids, thuốc dãn phế quản dạng hít, và thuốc giảm đau (aspirin, ibuprofen và paracetamol). Không thấy có sự thay đổi nào về phản ứng phụ hoặc tần suất xuất hiện các phản ứng phụ khi dùng Tamiflu chung với các thuốc này.
Tác dụng ngoại ý
Các thử nghiệm lâm sàng
Các nghiên cứu điều trị ở người trưởng thành
Trong các nghiên cứu pha III điều trị bệnh cúm ở người trưởng thành, người ta thấy trên tổng số 2107 bệnh nhân (gồm cả những bệnh nhân dùng giả dược và những bệnh nhân dùng Tamiflu 75mg, 2 lần mỗi ngày và Tamiflu 150mg 2 lần mỗi ngày), những phản ứng phụ thường gặp nhất là nôn và buồn nôn. Những biểu hiện này chỉ thoáng qua và nhìn chung, thường xảy ra khi dùng liều đầu tiên. Trong hầu hết các trường hợp, những biểu hiện này không dẫn đến việc phải ngưng dùng thuốc cho bênh nhân. Với liều 75mg 2 lần mỗi ngày, có 3 bệnh nhân phải ngưng dùng thuốc vì buồn nôn và 3 bệnh nhân khác phải ngưng dùng thuốc vì bị nôn.
Trong các nghiên cứu pha III điều trị bệnh cúm ở người trưởng thành, một vài tác dụng không mong muốn đã xảy ra thường xuyên hơn ở nhóm bệnh nhân dùng Tamiflu, so với nhóm bệnh nhân dùng giả dược. Với liều khuyên dùng, những tác dụng không mong muốn thường xuất hiện nhất được trình bày ở bảng 1. Bảng tóm tắt này bao gồm cả những người trưởng thành khỏe mạnh lẫn những bệnh nhân có nguy cơ (là những bệnh nhân có nguy cơ cao xuất hiện các biến chứng khi mắc bệnh cúm, ví dụ như người già, bệnh nhân bị bệnh tim hoặc bệnh phổi mãn tính). Những tác dụng không mong muốn có tỷ lệ ≥ 1% và được báo cáo thường xuyên hơn ở nhóm bệnh nhân dùng Tamiflu so với nhóm dùng giả dược, chưa xét đến mối quan hệ nhân quả, là: buồn nôn, nôn, đau bụng và nhức đầu.
Bảng 1: Những tác dụng không mong muốn thường gặp nhất trong các nghiên cứu về bệnh cúm mắc phải một cách tự nhiên
Các tác dụng không mong muốn Điều trị bệnh* Phòng bệnh
Giả dược N=1050 Oseltamivir 75mg hai lần mỗi ngày N=1057 Giả dược N=1434 Oseltamivir 75mg một lần mỗi ngày N=1480
Buồn nôn (không nôn) Nôn Tiêu chảy Viêm phế quản Đau bụng Choáng váng Nhức đầu Mất ngủ Ho*** Chóng mặt*** Mệt mỏi*** 71 (6,8%) 32 (3,0%) 84 (8,0%) 52 (5,0%) 21 (2,0%) 31 (3,0%) 16 (1,5%) 10 (1,0%) 12 (1,1%) 6 (0,6%) 7 (0,7%) 113 (10,7%) 85 (8,0%) 58 (5,5%) 39 (3,7%) 23 (2,2%) 20 (1,9%) 17 (1,6%) 11 (1,0%) 10 (0,9%) 9 (0,9%) 8 (0,8%) 56 (3,9%) 15 (1,0%) 38 (2,6%) 17 (1,2%) 23 (1,6%) 21 (1,5%) 251 (17,5%) 14 (1,0%) 86 (6,0%) 3 (0,2%) 107 (7,5%) 104 (7,0%) 31 (2,1%) 48 (3,2%) 11 (0,7%) 30 (2,0%) 24 (1,6%) 298 (20,1%) 18 (1,2%) 83 (5,6%) 4 (0,3%) 117 (7,9%)
* Các tác dụng không mong muốn được ghi nhận là tất cả các tác dụng không mong muốn hay gặp nhất trong các nghiên cứu điều trị ở nhóm dùng oseltamivir 75mg hai lần mỗi ngày, và các tác dụng không mong muốn này được sắp xếp theo tỉ lệ giảm dần trong nhóm đó.
Nói chung, dữ liệu về các tác dụng không mong muốn ở nhóm bệnh nhân có nguy cơ trong các nghiên cứu điều trị tương tự về mặt định tính so với nhóm người lớn khỏe mạnh.
Các nghiên cứu phòng bệnh cúm
Tổng số 3434 đối tượng (thanh thiếu niên, người trưởng thành khỏe mạnh và người già) tham gia trong các nghiên cứu pha III phòng bệnh cúm, trong đó có 1480 người được dùng liều khuyên dùng 75mg, ngày một lần trong 6 tuần. Các tác dụng không mong muốn, về mặt định tính, giống với những số liệu đã được ghi nhận trong các nghiên cứu điều trị, dù thời gian dùng thuốc kéo dài hơn (Bảng 1). Trong các nghiên cứu phòng bệnh cúm, những tác dụng không mong muốn đã được ghi nhận thường xuyên hơn ở nhóm bệnh nhân dùng Tamiflu, so với nhóm bệnh nhân dùng giả dược. Những tác dụng không mong muốn này cũng thường xảy ra hơn trong các nghiên cứu phòng bệnh cúm, so với các nghiên cứu điều trị bệnh cúm, bao gồm: đau nhức, chảy nước mũi, khó tiêu và nhiễm trùng đường hô hấp trên. Tuy nhiên, sự khác biệt về tỉ lệ xuất hiện những tác dụng không mong muốn này giữa nhóm dùng Tamiflu và nhóm dùng giả dược là ít hơn 1%. Khi so sánh giữa nhóm 942 người già dùng Tamiflu hoặc giả dược với nhóm đối tượng trẻ hơn, xét về đô an toàn, người ta thấy không có sự khác biệt có ý nghĩa về mặt lâm sàng giữa hai nhóm.
Các nghiên cứu trong điều trị bệnh nhi
Có tất cả 1032 trẻ từ 1 đến 12 tuổi (bao gồm 698 trẻ khoẻ mạnh, từ 1 đến 12 tuổi và 334 trẻ bị bệnh hen, từ 6 đến 12 tuổi) tham gia vào các nghiên cứu pha III dùng oseltamivir để điều trị bệnh cúm. Có 515 bé được dùng oseltamivir dạng huyền dịch.
Các tác dụng không mong muốn xảy ra > 1% ở nhóm trẻ được dùng oseltamivir, và được liệt kê trong Bảng 2. Tác dụng không mong muốn được báo cáo thường xuyên nhất là nôn. Những tác dụng khác cũng được báo cáo thường xuyên từ nhóm bé được điều trị với oseltamivir là: đau bụng, chảy máu cam, rối loạn về tai và viêm kết mạc. Nói chung, những tác dụng không mong muốn này chỉ xảy ra một lần, tự khỏi dù vẫn tiếp tục dùng thuốc và trong phần lớn các trường hợp, không dẫn đến kết quả là phải ngưng dùng thuốc.
Bảng 2: Các tác dụng không mong muốn thường xảy ra nhất ở những trẻ từ 1 đến 12 tuổi trong những thử nghiệm bệnh cúm mắc phải tự nhiên
Những tác dụng không mong muốn xảy ra trong quá trình điều trị ở > 1% bệnh nhi tham gia vào các thử nghiệm pha III điều trị bệnh cúm mắc phải tự nhiên bằng Tamiflu.
Điều trị bệnha Điều trị bệnhb Phòng bệnhb
Các tác dụng không mong muốn Giả dược N=517 Oseltamivir 2mg/kg 2 lần mỗi ngày N=515 Oseltamivir Liều chuẩnc N=158 Oseltamivir Liều chuẩnc N=99
Nôn Tiêu chảy Viêm tai giữa Đau bụng Hen (kể cả tình trạng nặng) Buồn nôn Chảy máu cam Viêm phổi Rối loạn về tai Viêm xoang Viêm phế quản Viêm kết mạc Viêm da Nổi hạch Rối loạn màng nhĩ 48 (9,3%) 55 (10,6%) 58 (11,2%) 20 (3,9%) 19 (3,7%) 22 (4,3%) 13 (2,5%) 17 (3,3%) 6 (1,2%) 13 (2,5%) 11 (2,1%) 2 (0,4%) 10 (1,9%) 8 (1,5%) 6 (1,2%) 77 (15,0%) 49 (9,5%) 45 (8,7%) 24 (4,7%) 18 (3,5%) 17 (3,3%) 16 (3,1%) 10 (1,9%) 9 (1,7%) 9 (1,7%) 8 (1,6%) 5 (1,0%) 5 (1,0%) 5 (1,0%) 5 (1,0%) 31 (19,6%) 5 (3,2%) 2 (1,3%) 3 (1,9%) – 10 6,3%) 2 (1,3%) – – – 3 (1,9%) – 1 (0,6%) 1 (0,6%) – 10 (10,1%) 1 (1,0%) 2 (2,0%) 3 (3,0%) 1 (1,0%) 4 (4,0%) 1 (1,0%) – – – – – – – –
a Dữ liệu thu nhập được từ các thử nghiệm pha III điều trị bệnh cúm mắc phải tự nhiên bằng Tamiflu.
b Thử nghiệm không có chứng so sánh giữa điều trị bệnh (liều 2 lần mỗi ngày, trong 5 ngày) và phòng bệnh (liều 1 lần mỗi ngày, trong 10 ngày)
c Liều chuẩn = liều được tính dựa trên tuổi (Xem mục Liều lượng và cách sử dụng)
Những tác dụng không mong muốn được xét đến ở đây bao gồm: những tác dụng xảy ra trong các thử nghiệm điều trị bệnh có tần số xuất hiện ≥ 1% ở nhóm được điều trị với oseltamivir 75mg, 2 lần mỗi ngày.
Phòng ngừa ở bệnh nhi
Những bệnh nhi từ 1 đến 12 tuổi tham gia vào thử nghiệm để phòng bệnh cúm sau khi tiếp xúc với nguồn bệnh. Thử nghiệm này được tiến hành tại nhà với cả những trường hợp chỉ điểm (n=134) lẫn những trường hợp tiếp xúc (n=222). Những tác dụng trên đường tiêu hoá thường xảy ra nhiều nhất, đặc biệt là nôn. Trong thử nghiệm này, Tamiflu được dung nạp rất tốt và những tác dụng không mong muốn được ghi nhận ở đây hoàn toàn phù hợp với những tác dụng đã được quan sát thấy từ trước (xem bảng 2)
Sau khi lưu hành thuốc
Rối loạn da và tổ chức dưới da: Hiếm có các trường hợp có các phản ứng quá mẫn như là các phản ứng da dị ứng bao gồm viêm da, phát ban, chàm, mề đay; và rất hiếm các trường hợp như ban đỏ đa dạng, hội chứng Stevens-Johnson và hoại tử biểu bì do độc tố đã được ghi nhận. Các trường hợp dị ứng, phản ứng phản vệ và phù mặt cũng hiếm khi được báo cáo.
Rối loạn gan và hệ thống đường mật: rất hiếm gặp các trường hợp viêm gan và các men gan tăng cao ở những bệnh nhân bị ốm giả cúm được điều trị bằng oseltamivir.
Rối loạn tâm thần/Rối loạn hệ thần kinh: Co giật và mê sảng (bao gồm các triệu chứng như thay đổi ý thức, nhầm lẫn, hành vi bất thường, ảo tưởng, ảo giác, bồn chồn, lo lắng, ác mộng) đã được ghi nhận ở những bệnh nhân cúm dùng Tamiflu, chủ yếu xảy ra ở trẻ em và thanh thiếu niên. Trong một vài trường hợp rất hiếm gặp, tình trạng mê sảng này có thể gây nên chấn thương do tai nạn. Hiện vẫn chưa biết rõ được vai trò của Tamiflu đối với các biến cố này. Những tác dụng trên tâm thần kinh này cũng đã được ghi nhận ở những bệnh nhân bị bệnh cúm mà không dùng Tamiflu.
Rối loạn tiêu hóa: trong một vài trường hợp hiếm xuất huyết tiêu hóa được quan sát thấy sau khi sử dụng Tamiflu. Đặc biệt viêm đại tràng xuất huyết đã được báo cáo và thuyên giảm sau khi rút ngắn thời gian điều trị cúm với Tamiflu hoặc ngưng thuốc.
Liều lượng và cách dùng
Tamiflu có thể được dùng kèm hoặc không kèm theo thức ăn. (Xem mục Dược động học). Tuy nhiên, dùng Tamiflu kèm với thức ăn có thể làm tăng khả năng dung nạp thuốc ở một số bệnh nhân.
Trong trường hợp hỗn dịch uống Tamiflu không sẵn có, người lớn, thanh thiếu niên và trẻ em không thể nuốt viên thuốc, có thể uống Tamiflu bằng cách mở viên nang và cho toàn bộ lượng thuốc trong viên nang vào một lượng vừa đủ (tối đa 1 thìa cà phê) thức uống ngọt như siro chocolate thường hoặc loại không đường, mật ong (chỉ dành cho trẻ em trên hai tuổi), đường nâu sáng hoặc đường tinh khiết hoà tan trong nước, kem tươi, sữa đặc có đường, nước sốt táo hoặc sữa chua để che giấu vị đắng của thuốc. Khuấy đều hỗn hợp và đưa cho bệnh nhân. Cần uống hỗn hợp này ngay sau khi pha chế.
Liều chuẩn:
Điều trị bệnh cúm
Nên bắt đầu điều trị vào ngày thứ nhất hoặc ngày thứ hai khi xuất hiện các triệu chứng đầu tiên của bệnh cúm
Người lớn và thanh thiếu niên:
Ở người lớn và thiếu niên từ 13 tuổi trở lên, liều khuyên dùng là uống viên nang Tamiflu 75mg hai lần mỗi ngày, trong 5 ngày. Trong trường hợp không thể nuốt được viên nang, có thể dùng dạng huyền dịch với liều 75mg Tamiflu hai lần mỗi ngày, trong 5 ngày.
Trẻ em:
Trẻ có cân nặng trên 40kg nếu có thể nuốt được viên nang, cũng sẽ được điều trị với liều uống viên nang 75mg hai lần mỗi ngày, thay vì dùng Tamiflu dạng huyền dịch với liều khuyên dùng như bảng dưới đây:
Liều uống được khuyên dùng của Tamiflu cho trẻ từ một tuổi trở lên:
Trọng lượng cơ thể Liều khuyên dùng trong 5 ngày
≤ 15kg 30 mg hai lần mỗi ngày
> 15kg đến 23kg 45 mg hai lần mỗi ngày
> 23kg đến 40kg 60 mg hai lần mỗi ngày
> 40kg 75 mg hai lần mỗi ngày
Có sẵn bơm định liều được đánh dấu các mức liều dùng 30mg, 45mg và 60mg cho dạng huyền dịch uống
Tamiflu dạng bột pha huyền dịch uống nên được pha chế bởi dược sĩ trước khi dùng cho bệnh nhân (Xem mục Hướng dẫn đặc biệt cho việc sử dụng và tiêu hủy thuốc)
Phòng ngừa bệnh cúm
Người lớn và thanh thiếu niên:
Liều khuyên dùng để phòng ngừa bệnh cúm là sau khi tiếp xúc với người bị nhiễm cúm, nên uống Tamiflu 75mg ngày một lần, trong 10 ngày. Nên bắt đầu việc điều trị trong vòng hai ngày sau khi tiếp xúc với nguồn bệnh. Liều khuyên dùng để phòng bệnh cúm trong suốt thời gian có dịch ở cộng đồng là dùng 75mg ngày một lần. Tính an toàn và hiệu quả của việc dùng thuốc đã được chứng minh cho tới 6 tuần. Chừng nào vẫn còn dùng thuốc thì thời gian bảo vệ của thuốc vẫn còn.
Trẻ em:
Trẻ có cân nặng trên 40kg nếu có thể nuốt được viên nang, sẽ được điều trị phòng bệnh cúm với viên nang 75mg, uống ngày một lần, trong 10 ngày, thay vì dùng Tamiflu dạng huyền dịch với liều khuyên dùng như bảng dưới đây:
Liều uống được khuyên dùng của Tamiflu để phòng ngừa bệnh cúm cho trẻ từ một tuổi trở lên:
Trọng lượng cơ thể Liều khuyên dùng trong 10 ngày
≤ 15kg 30 mg ngày một lần
> 15kg đến 23kg 45 mg ngày một lần
> 23kg đến 40kg 60 mg ngày một lần
> 40kg 75 mg ngày một lần
Có sẵn bơm định liều đánh dấu các mức liều dùng 30mg, 45mg và 60mg cho dạng huyền dịch uống
Tamiflu dạng bột pha huyền dịch uống nên được pha chế bởi dược sĩ trước khi dùng cho bệnh nhân (Xem mục Hướng dẫn đặc biệt cho việc sử dụng và tiêu hủy thuốc)
Những hướng dẫn liều đặc biệt:
Bệnh nhân suy thận
Điều trị bệnh cúm
Không cần điều chỉnh liều cho những bệnh nhân có độ thanh thải creatinine trên 30 ml/phút. Ở những bệnh nhân có độ thanh thải creatinine từ 10-30 ml/phút, cần giảm liều Tamiflu xuống 75mg uống ngày một lần, trong 5 ngày. Không có liều khuyên dùng cho những bệnh nhân bị bệnh thận giai đoạn cuối đang được lọc máu thường qui và thẩm phân phúc mạc liên tục, cũng như những bệnh nhân có độ thanh thải creatinine ≤ 10 ml/phút (Xem mục Dược động học ở những đối tượng đặc biệt và mục Chú ý đề phòng và Thận trọng lúc dùng)
Phòng ngừa bệnh cúm
Không cần điều chỉnh liều cho những bệnh nhân có độ thanh thải creatinine trên 30 ml/phút. Ở những bệnh nhân có độ thanh thải creatinine từ 10-30 ml/phút, liều dùng nên được giảm xuống còn 75mg Tamiflu, cách một ngày uống một lần, hoặc uống 30mg dạng huyền dịch ngày một lần. Không có liều khuyên dùng cho những bệnh nhân bị bệnh thận giai đoạn cuối đang được lọc máu thường qui và thẩm phân phúc mạc liên tục, cũng như những bệnh nhân có độ thanh thải creatinine ≤ 10 ml/phút (Xem mục Dược động học ở những đối tượng đặc biệt và mục Chú ý đề phòng và Thận trọng lúc dùng)
Bệnh nhân suy gan
Không cần điều chỉnh liều cho những bệnh nhân bị rối loạn chức năng gan vừa hoặc nhẹ khi được điều trị hoặc phòng ngừa bệnh cúm (Xem mục Dược động học ở những đối tượng đặc biệt). Độ an toàn và đặc tính dược động học ở bệnh nhân suy gan nặng chưa được nghiên cứu
Người già
Không cần điều chỉnh liều cho người già khi được điều trị hoặc phòng ngừa bệnh cúm (Xem mục Dược động học ở những đối tượng đặc biệt)
Trẻ em
Tính an toàn và hiệu quả của Tamiflu ở trẻ dưới một tuổi chưa được xác lập (Xem mục Dược động học ở những đối tượng đặc biệt). Không nên dùng Tamiflu cho trẻ dưới một tuổi (Xem mục An toàn tiền lâm sàng).
Cách sử dụng và hủy bỏ
Chuẩn bị bột Tamiflu cho dạng huyền dịch uống
Người ta khuyến cáo rằng bột Tamiflu cho dạng huyền dịch uống nên được pha bởi dược sĩ trước khi đưa cho bệnh nhân (Xem mục Liều lượng và Cách dùng):
1. Vỗ vào lọ thuốc đóng kín vài lần để thuốc tơi ra.
2. Đong 52 ml nước. Sử dụng cốc lường nước (được cung cấp sẵn) và đong nước đến mức đã chỉ định.
3. Đổ 52 ml nước để pha thuốc vào lọ thuốc và lắc kỹ lọ thuốc đã được đóng kín trong 15 giây.
4. Mở nắp lọ thuốc (loại bảo vệ không cho trẻ mở) và ấn bộ phận tiếp hợp vào cổ lọ thuốc.
5. Đóng nắp bảo vệ lọ thuốc lại thật chặt. Điều này giúp cố định đúng chỗ bộ phận tiếp hợp ở lọ thuốc và khả năng bảo vệ của nắp lọ thuốc.
Tờ hướng dẫn sử dụng và ống lấy thuốc sẽ được đưa cho bệnh nhân. Nên viết ngày hết hạn của huyền dịch đã pha trên nhãn thuốc.
Quá liều
Hiện nay vẫn chưa có kinh nghiệm về sử dụng quá liều, tuy nhiên, những biểu hiện có thể dự đoán được của tình trạng quá liều cấp tính là buồn nôn, có hoặc không kèm theo nôn mửa. Liều đơn tới 1000mg Tamiflu vẫn được dung nạp tốt, ngoại trừ triệu chứng buồn nôn và/hoặc nôn.
Bảo quản
Viên nang: không bảo quản thuốc ở nhiệt độ trên 25oC.
Bột pha huyền dịch uống: không bảo quản thuốc ở nhiệt độ trên 25oC.
Huyền dịch đã được pha: bảo quản trong vòng 10 ngày, không bảo quản thuốc ở nhiệt độ trên 25oC hoặc 17 ngày, ở nhiệt độ 2-8oC (trong ngăn mát tủ lạnh).
Nguồn: Vidal Việt Nam 2012






Reviews
There are no reviews yet.