THUỐC IRESSA ĐIỀU TRỊ UNG THƯ PHỔI GIÁ BAO NHIÊU? MUA Ở ĐÂU CHÍNH HÃNG?
Liên hệ để biết giá !
Nội dung mô tả tóm tắt:
THUỐC IRESSA ĐIỀU TRỊ UNG THƯ PHỔI GIÁ BAO NHIÊU? MUA Ở ĐÂU CHÍNH HÃNG?
Thuốc Iressa 250mg chứa hoạt chất Gefitinib do hãng Astrazeneca ngiên cứu sản xuất và phân phối tại Việt Nam. Thuốc Iresa 250mg là 1 thuốc kê đơn được chỉ định để điều trị những người bị ung thư phổi không phải tế bào nhỏ (NSCLC). Đã lan sang các phần khác của cơ thể và Có một số loại gen thụ thể yếu tố biểu hiện tăng trưởng bất thường (EGFR), và những người chưa từng điều trị ung thư
Thông tin thuốc
Tên thuốc: Iressa
Thành phần: Gefitinib
Hàm lượng: 250mg
Nhà sản xuất: công ty Astrazeneca
Quy cách: hộp 30 viên
THÔNG TIN THÀNH PHẦN CÓ TRONG THUỐC IRESSA
Thành phần: Gefitinib 250mg
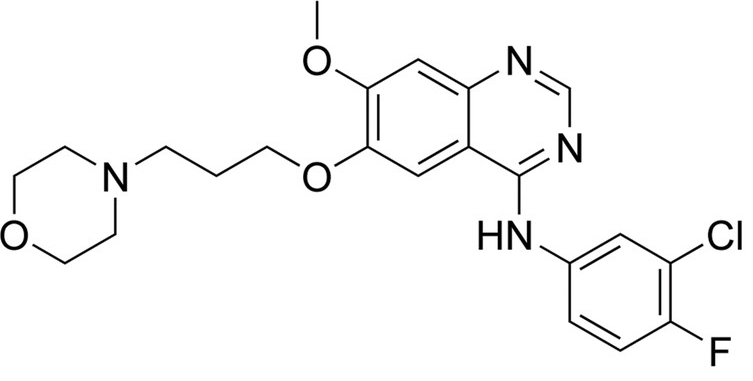
Ngày 13 tháng 7 năm 2015 thuốc iressa 250mg (gefitinib 250mg) được FDA xem như một phương pháp điều trị đầu tiên ở những bệnh nhân ung thư phổi tế bào không di căn nhỏ (NSCLC) có khối u có thụ thể yếu tố tăng trưởng biểu bì (EGFR) exon 19 xóa hoặc exon 21 (L858R).
Iressa được chấp thuận ở 91 quốc gia để điều trị bệnh nhân người lớn với NSCLC đột biến EGFR đột biến di căn.
Cơ chế hoạt động
Gefitinib là chất ức chế chọn lọc đầu tiên của miền tyrosine kinase của yếu tố tăng trưởng biểu bì (EGFR) . Do đó gefitinib là một chất ức chế EGFR . Protein mục tiêu (EGFR) là thành viên của một họ thụ thể ( ErbB ) bao gồm Her1 (EGFR), Her2 (erb-B2), Her3 (erb-B3) và Her4 (Erb-B4). EGFR được biểu hiện quá mức trong các tế bào của một số loại ung thư biểu mô ở người – ví dụ như trong ung thư phổi và ung thư vú. Điều này dẫn đến việc kích hoạt không phù hợp của tầng tín hiệu Ras chống apoptotic , cuối cùng dẫn đến sự tăng sinh tế bào không kiểm soát được. Nghiên cứu về ung thư phổi không tế bào nhỏ nhạy cảm với gefitinibđã chỉ ra rằng một đột biến trong miền EGFR tyrosine kinase chịu trách nhiệm kích hoạt các con đường chống apoptotic. Những đột biến này có xu hướng làm tăng độ nhạy cảm với các thuốc ức chế tyrosine kinase như gefitinib và erlotinib. Trong số các loại mô học ung thư phổi không phải tế bào nhỏ, ung thư biểu mô tuyến là loại thường xuyên nhất chứa chấp những đột biến này. Những đột biến này thường thấy ở người châu Á, phụ nữ và những người không hút thuốc (những người cũng có xu hướng thường mắc ung thư tuyến).
Gefitinib ức chế EGFR tyrosine kinase bằng cách liên kết với vị trí gắn adenosine triphosphate (ATP) của enzyme. Do đó, chức năng của EGFR tyrosine kinase trong việc kích hoạt tầng tải tín hiệu Ras chống apoptotic bị ức chế, và các tế bào ác tính bị ức chế.
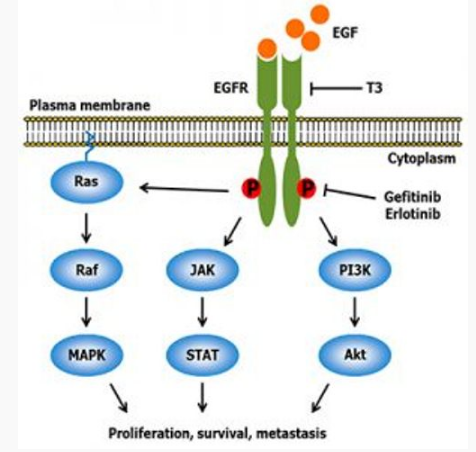
CHỈ ĐỊNH CỦA THUỐC IRESSA
Thuốc Iressa 250mg được chỉ định điều trị cho bệnh nhân ung thư phổi loại không phải tế bào nhỏ (Non Small Cell Lung Cancer-NSCLC) giai đoạn tiến triển tại chỗ hoặc di căn mà trước đây đã dùng hóa trị liệu hoặc không thích hợp để hóa trị liệu.
CHỐNG CHỈ ĐỊNH
Chống chỉ định với bệnh nhân mẫn cảm với thành phần trong Thuốc iressa.
Phụ nữ đang mang thai và cho con bú: cần có sự tư vấn đánh giá của bác sĩ điều trị.
TÁC DỤNG KHÔNG MONG MUỐN
Tác dụng phụ thường gặp nhất (ADR xảy ra ở hơn 20% bệnh nhân ) là tiêu chảy và phản ứng da ( bao gồm phát ban, mụn trứng cá, da khô và ngứa).
Tác dụng phụ thường xảy ra trong tháng điều trị đầu tiên và thường có thể đảo ngược.
Khoảng 8% bệnh nhân gặp phải nhiều tắc dụng phụ nặng hơn trên mắt, gan thận, máu.
Khoảng 3% bệnh nhân ngừng điều trị do tác dụng phụ kéo dài.
Bệnh phổi kẽ (ILD) đã xảy ra ở 1,3% bệnh nhân, thường nặng. Cần theo dõi ngừng thuốc nếu bệnh có diễn biến phức tạp.
Khuyến cáo không sử dụng thuốc trên phụ nữ mang thai và cho con bú.
Trong thời gian điều trị với gefitinib gây suy nhược cơ thể. Do đó nên thận trọng khi lái xe hoặc sử dụng máy móc.
HƯỚNG DẪN SỬ DỤNG
Liều dùng
Liều khuyến cáo của thuốc IRESSA 250mg là 250 mg. Mỗi ngày một lần cho đến khi bệnh tiến triển hoặc độc tính không thể chấp nhận
Chọn bệnh nhân để điều trị đầu tiên của NSCLC di căn với IRESSA. Dựa trên sự hiện diện của EGFR exon 19 xóa hoặc exon 21 (L858R) đột biến thay thế trong khối u của họ.
Cách dùng
Thuốc Iressa 250mg được sử dụng trước ăn hoặc sau ăn. Có thể hòa tan thuốc Iressa vào 4-8ml nước.
Sau đấy uống và tráng lại cốc và uống hết thuốc.
LƯU Ý TRƯỚC KHI SỬ DỤNG THUỐC
Trước khi sử dụng thuốc điều trị ung thư Iressa 250mg Gefitinib
Có vấn đề về phổi hoặc hô hấp
Từng có vấn đề về gan
Có vấn đề thị giác hoặc mắt
Đang mang thai hoặc dự định có thai. IRESSA có thể gây hại cho thai nhi của bạn.
Phụ nữ có khả năng mang thai nên sử dụng phương pháp ngừa thai hiệu quả trong khi điều trị với IRESSA và trong ít nhất 2 tuần sau liều thuốc IRESSA 250mg cuối cùng.
Bạn nên tránh mang thai trong khi điều trị với thuốc IRESSA 250mg.
Báo cho bác sĩ của bạn ngay lập tức nếu bạn có thai trong khi điều trị với thuốc IRESSA 250mg
đang cho con bú hoặc dự định cho con bú.
Chưa có nghiên cứu thuốc IRESSA 250mg GEFITINIB đi vào sữa mẹ. Không cho con bú trong khi điều trị với thuốc IRESSA 250mg.
Nói chuyện với nhà cung cấp dịch vụ chăm sóc sức khỏe của bạn về cách tốt nhất để cho bé bú trong thời gian này.
Báo cho bác sĩ của bạn biết về tất cả các loại thuốc bạn uống. Bao gồm thuốc theo toa và thuốc không kê đơn, vitamin hoặc thuốc bổ thảo dược.
Nếu bạn dùng thuốc ức chế bơm proton (PPI), thuốc chẹn H2 hoặc thuốc kháng acid. Hãy nói chuyện với bác sĩ của bạn về thời gian tốt nhất để dùng thuốc trong khi điều trị với IRESSA.
Nếu quý vị uống thuốc làm loãng máu gọi là warfarin. Nên làm xét nghiệm máu thường xuyên để kiểm tra mức độ đông máu của quý vị trong thời gian điều trị với thuốc IRESSA 250mg.
MUA THUỐC IRESSA Ở ĐÂU? GIÁ BAO NHIÊU?
Thuốc Iressa là thuốc gì? Thuốc Iressa mua ở đâu chính hãng? Giá thuốc Iressa bao nhiêu? Công dụng thuốc Iressa là gì? Thuốc Iressa có tốt không? Thuốc Iressa trên đây là các câu hỏi mà bạn đọc hay gặp phải, để được tư vấn về giá, địa chỉ mua thuốc Iressa chính hãng giá rẻ nhât xin LH Ds Dũng 0978.342.324 để được tư vấn.Thuốc Iressa có bán tại hệ thống thuockedon24h.com, với giá rẻ nhất giao hàng toàn quốc.
Văn Tuấn
THÔNG TIN THÀNH PHẦN XELODA
Thành phần: Capecitabine
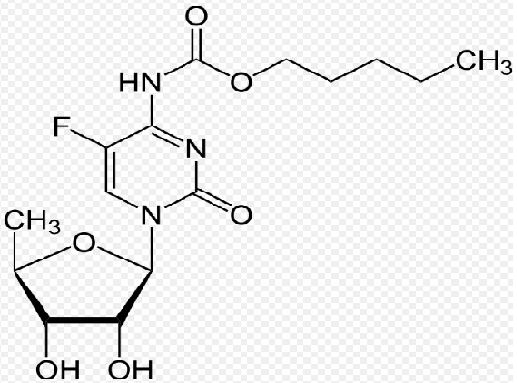
Capecitabine thuộc về một nhóm thuốc gọi là thuốc chống dị ứng
Capecitabine được sử dụng để điều trị ung thư ruột kết, và ung thư vú hoặc ung thư đại trực tràng đã lan sang các bộ phận khác của cơ thể.
Capecitabine thường được sử dụng kết hợp với các loại thuốc điều trị ung thư khác hoặc phương pháp điều trị bức xạ.
Cơ chế tác dụng
Capecitabine là dẫn xuất fluoropyrimidine carbamate được điều chế để dùng đường uống, là thuốc độc tế bào được hoạt hóa bởi khối u và chọn lọc trên khối u.
Capecitabine không phải là chất độc tế bào trên in vitro. Tuy nhiên, trên in vivo, thuốc được biến đổi liên tiếp thành chất gốc độc tế bào là 5-fluorouracil (5-FU), chất này sẽ được chuyển hoá tiếp.
Sự hình thành 5-FU tại khối u nhờ xúc tác một cách tối ưu của yếu tố tạo mạch liên quan tới khối u là thymidine phosphorylase (dThdPase), nhờ đó làm giảm tối đa mức độ của mô lành với 5-FU trong cơ thể.
Sự biến đổi sinh học tuần tự của men từ capecitabine thành 5-FU dẫn tới nồng độ của 5-FU cao hơn trong mô khối u. Sau khi cho bệnh nhân bị ung thư đại trực tràng (N=8) uống capecitabine, tỉ số nồng độ của 5FU ở khối u đại trực tràng so với các mô gần kề là 3,2 (dao động từ 0,9 đến 8,0). Tỉ số nồng độ ở khối u so với huyết tương là 21,4 (dao động từ 3,9 đến 59,9) trong khi tỉ số ở các mô khỏe mạnh so với huyết tương là 8,9 (dao động từ 3,0 đến 25,8). Hoạt tính của thymidine phosphorylase cao hơn gấp 4 lần ở khối u đại trực tràng so với mô bình thường bên cạnh.
Bệnh nhân ung thư vú, dạ dày, đại trực tràng, cổ tử cung, và buồng trứng có nồng độ thymidine phosphorylase cao hơn (có khả năng chuyển 5′-DFUR [5′-deoxy-5-fluorouridine] thành 5-FU) so với các mô bình thường tương ứng.
Các tế bào bình thường và các tế bào khối u chuyển hóa 5-FU thành 5-fluoro-2-deoxyuridine monophosphate (FdUMP) và 5-fluorouridine triphosphate (FUTP). Những chất chuyển hóa này sẽ làm tổn thương tế bào bằng hai cơ chế. Đầu tiên, FdUMP và đồng yếu tố folate N5-10-methylenetetrahydrofolate gắn với thymidylate synthase (TS) tạo nên một phức hợp gồm ba yếu tố đồng hoá trị.
Sự gắn kết này sẽ ức chế sự hình thành thymidylate từ uracil. Thymidylate là một tiền chất cần thiết của thymidine triphosphate, một chất cần thiết cho sự tổng hợp DNA, vì vậy sự thiếu hụt hợp chất này có thể ức chế sự phân chia tế bào. Thứ hai, các men sao chép nhân có thể kết hợp một cách nhầm lẫn FUTP thay vì uridine triphosphate (UTP) trong quá trình tổng hợp RNA. Lỗi chuyển hóa này có thể ảnh hưởng tới sự tổng hợp RNA và protein trong quá trình phát triển của tế bào ung thư.
Dược động học
Hấp thu
Sau khi uống, capecitabine được hấp thu nhanh chóng và rộng khắp, sau đó được chuyển hoá mạnh thành chất chuyển hóa 5′-deoxy-5-fluorocytidine (5′-DFCR) và 5’DFUR. Dùng cùng với thức ăn làm giảm tỉ lệ hấp thu capecitabine, nhưng chỉ ảnh hưởng rất ít.
Phân phối
Gắn kết với Protein. Các nghiên cứu huyết tương trên in-vitro đã chứng minh rằng tỉ lệ gắn kết protein của capecitabine, 5′-DFCR, 5′-DFUR và 5-FU lần lượt là 54%, 10%, 62% và 10%, chủ yếu gắn với albumin.
Chuyển hóa
Capecitabineđược chuyển hóa đầu tiên bởi men carboxylesterase ở gan thành 5′-DFCR, chất này sau đó được chuyển thành 5′-DFUR bởi cytidine deaminase, là men tập trung chủ yếu ở gan và mô khối u.
Sự hình thành 5-FU xảy ra chủ yếu tại vị trí khối u bởi yếu tố tạo mạch có liên quan đến khối u là dThdPase, do đó làm giảm tối đa mức độ của mô lành với 5-FU trong cơ thể. AUC huyết tương của 5-FU thấp hơn 6 đến 22 lần nồng độ sau khi truyền tĩnh mạch nhanh 5-FU (liều 600mg/m2). Các chất chuyển hóa của capecitabine chỉ trở nên có độc tính sau khi chuyển thành 5-FU và các chất đồng hóa của 5-FU (xem phần Cơ chế hoạt động).
5-FU được chuyển hóa tiếp thành các chất chuyển hóa không có hoạt tính dihydro-5-fluoruracil (FUH2), 5 fluoro-ureidopropionic acid (FUPA) và á-fluoro-â-alanine (FBAL) thông qua dihydropyrimidine dehydrogenase (DPD), chất này mang tính chuyển hóa chậm.
Đào thải
Thời gian bán thải (t1/2 tính bằng giờ) của capecitabine, 5′-DFCR, 5′-DFUR, 5 FU và FBAL tương ứng là 0.85, 1.11, 0.66, 0.76 và 3.23. Dược động học của capecitabine được đánh giá trên khoảng liều là 502-3514mg/m2/ngày. Các thông số của capecitabine, 5′-DFCR và 5′-DFUR được đo vào ngày đầu tiên và ngày 14 là như nhau. AUC của 5-FU là 30%-35% cao hơn vào ngày 14, nhưng không tăng lên sau đó (ngày 22). Tại liều điều trị, dược động học của capecitabine và các chất chuyển hoá của nó tỉ lệ với liều, trừ 5-FU.
Sau khi uống, các chất chuyển hóa của capecitabine được tìm thấy chủ yếu trong nước tiểu. 95.5% liều capecitabine được dùng tìm thấy trong nước tiểu. Bài tiết trong phân rất ít (2,6%). Chất chuyển hóa chính có trong nước tiểu là FBAL, chiếm 57% liều dùng. Khoảng 3% liều dùng được đào thải trong nước tiểu dưới dạng thuốc không đổi.
CHỈ ĐỊNH CỦA THUỐC XELODA
Ung thư vú
Xeloda được chỉ định phối hợp với docetaxel để điều trị những bệnh nhân ung thư vú tiến triển tại chỗ hoặc di căn sau khi thất bại với hóa trị liệu độc tế bào. Liệu pháp điều trị trước đây bao gồm anthracycline. Xeloda cũng được chỉ định như đơn trị liệu cho điều trị những bệnh nhân ung thư vú tiến triển tại chỗ hoặc di căn sau khi thất bại với chế độ hóa trị bao gồm anthracycline và taxane hoặc cho những ung thư khác mà không có chỉ định dùng anthracycline.
Ung thư đại trực tràng
Xeloda được chỉ định điều trị hỗ trợ cho những bệnh nhân ung thư đại tràng sau phẫu thuật.
Xeloda còn được dùng để điều trị cho những bệnh nhân ung thư đại trực tràng di căn.
Ung thư dạ dày
Xeloda phối hợp với hợp chất platin được chỉ định điều trị bước một cho những bệnh nhân ung thư dạ dày tiến triển.
CHỐNG CHỈ ĐỊNH
Xeloda được chống chỉ định trên những bệnh nhân được biết là quá mẫn với capecitabine hoặc với bất kỳ thành phần nào của thuốc.
Xeloda được chống chỉ định trên những bệnh nhân có tiền sử các phản ứng nghiêm trọng và không dự đoán trước với fluoropyrimidine hoặc được biết là quá mẫn với fluorouracil.
Cũng như các fluoropyrimidine, Xeloda được chống chỉ định trên những bệnh nhân được biết là có thiếu hụt DPD (dihydropyrimidine dehydrogenase).
Không nên dùng Xeloda cùng với sorivudine hoặc các chất tương tự có liên quan về mặt hóa học, như là brivudine (xem phần Tương tác thuốc).
Xeloda được chống chỉ định trên những bệnh nhân bị suy gan nặng (Child Pugh C)
Xeloda được chống chỉ định trên những bệnh nhân bị suy thận nặng (độ thanh thải creatinine giảm dưới 30 ml/phút).
Nếu có chống chỉ định của bất kỳ thuốc nào trong điều trị kết hợp, thì không dùng thuốc đó.
TÁC DỤNG KHÔNG MONG MUỐN
Tác dụng phụ Xeloda phổ biến có thể bao gồm:
đau dạ dày hoặc khó chịu, táo bón; cảm giác mệt mỏi; phát ban da nhẹ; hoặc là tê hoặc ngứa ran ở tay hoặc chân của bạn.
Gọi cho bác sĩ của bạn ngay lập tức nếu bạn có: dấu hiệu phản ứng dị ứng với Xeloda: nổi mề đay; khó thở; sưng mặt, môi, lưỡi hoặc cổ họng của bạn.
buồn nôn, chán ăn, ăn ít hơn bình thường, nôn (nhiều hơn một lần trong 24 giờ);
tiêu chảy nặng (hơn 4 lần mỗi ngày, hoặc vào ban đêm);
phồng rộp hoặc loét trong miệng, nướu đỏ hoặc sưng, khó nuốt;
đau, đỏ, sưng, phồng rộp hoặc bong tróc da ở tay hoặc chân của bạn;
triệu chứng mất nước – cảm thấy rất khát hoặc nóng, không thể đi tiểu, đổ mồ hôi nhiều, hoặc da nóng và khô;
vấn đề về tim: đau ngực hoặc áp lực, nhịp tim không đều, khó thở ngay cả khi gắng sức nhẹ, sưng hoặc tăng cân nhanh;
vấn đề về thận: ít hoặc không đi tiểu; đi tiểu đau hoặc khó khăn; sưng ở bàn chân hoặc mắt cá chân của bạn; cảm thấy mệt mỏi hoặc khó thở;
các vấn đề về gan: buồn nôn, đau dạ dày trên, ngứa, cảm giác mệt mỏi, chán ăn, nước tiểu sẫm màu, phân màu đất sét, vàng da;
số lượng tế bào máu thấp: sốt hoặc các triệu chứng cúm khác, ho, lở da, da nhợt nhạt, dễ bầm tím, chảy máu bất thường, cảm thấy nhẹ đầu, nhịp tim nhanh; hoặc là
phản ứng da nghiêm trọng: sốt, đau họng, sưng ở mặt hoặc lưỡi, nóng rát ở mắt, đau da, sau đó là phát ban da đỏ hoặc tím lan rộng đặc biệt là ở mặt hoặc trên cơ thể và gây phồng rộp và bong tróc.
HƯỚNG DẪN SỬ DỤNG
Liều dùng
Bệnh nhân ung thư đại trực tràng, ung thư vú 1250 mg/m2, 2 lần/ngày (sáng, tối) x 14 ngày, sau đó là 7 ngày nghỉ thuốc.
Bệnh nhân điều trị kết hợp: Ung thư vú khởi đầu 1250 mg/m2, 2 lần/ngày x 2 tuần, phối hợp docetaxel, sau đó lá 1 tuần nghỉ;
Ung thư dạ dày, ung thư đại trực tràng 800-1000 mg/m2/lần x 2 lần/ngày x 2 tuần, sau đó 7 ngày nghỉ thuốc hoặc 625 mg/m2/lần x 2 lần/ngày khi điều trị liên tục.
Cách dùng:
Nên dùng thuốc Xeloda cùng với thức ăn: Uống với nước trong vòng 30 phút sau ăn.Chống chỉ định: Tiền sử phản ứng nghiêm trọng & không dự đoán trước với fluoropyrimidine hoặc quá mẫn với fluorouracil. Thiếu hụt DPD. Suy gan/thận nặng.
TƯƠNG TÁC THUỐC
Hãy thông báo với bác sĩ nếu bạn đang sử dụng những thuốc sau:
thuốc điều trị bệnh gút (allopurinol),
thuốc làm loãng máu (coumarin, warfarin),
một số loại thuốc chống vi-rút (sorivudine và brivudine),
thuốc trị co giật hoặc run (phenytoin),
interferon alpha,
xạ trị và một số loại thuốc dùng để điều trị ung thư (axit folinic, oxaliplatin, bevacizumab, cisplatin, irinotecan),
thuốc dùng để điều trị thiếu axit folic.
MUA THUỐC XELODA Ở ĐÂU? GIÁ BAO NHIÊU?
Thuốc Xeloda là thuốc gì? Thuốc Xeloda mua ở đâu chính hãng? Giá thuốc Xeloda bao nhiêu? Công dụng thuốc Xeloda là gì? Thuốc Xeloda có tốt không? Thuốc Xeloda trên đây là các câu hỏi mà bạn đọc hay gặp phải, để được tư vấn về giá, địa chỉ mua thuốc Xeloda chính hãng giá rẻ nhât xin LH Ds Dũng 0978.342.324 để được tư vấn.Thuốc Xeloda có bán tại hệ thống thuockedon24h.com, với giá rẻ nhất giao hàng toàn quốc.
Văn Tuấn
THUỐC XELODA ĐIỀU TRỊ UNG THƯ VÚ, UNG THƯ ĐẠI TRÀNG, UNG THƯ DẠ DÀY GIÁ BAO NHIÊU?
Thuốc Xeloda là thuốc nhóm Capecitabine chứa hóa chất fluoropyrimidine carbamate. Thuốc Xeloda được chỉ định điều trị cho những bệnh nhân mắc phải những căn bệnh ung thư như là bệnh ung thư đại trực tràng, ung thư dạ dày và ung thư vú
Thông tin thuốc
Tên thương hiệu: Xeloda
Thành phần hoạt chất: Capecitabine
Hãng sản xuất: ROCHE, THỤY SĨ
Hàm lượng: 150mg, 500mg
Dạng: Viên nén
Quy cách: viên nén 150mg hộp 60 viên, Viên nén 500mg hộp 120 viên
THÔNG TIN THÀNH PHẦN XELODA
Thành phần: Capecitabine
Capecitabine thuộc về một nhóm thuốc gọi là thuốc chống dị ứng
Capecitabine được sử dụng để điều trị ung thư ruột kết, và ung thư vú hoặc ung thư đại trực tràng đã lan sang các bộ phận khác của cơ thể.
Capecitabine thường được sử dụng kết hợp với các loại thuốc điều trị ung thư khác hoặc phương pháp điều trị bức xạ.
Cơ chế tác dụng
Capecitabine là dẫn xuất fluoropyrimidine carbamate được điều chế để dùng đường uống, là thuốc độc tế bào được hoạt hóa bởi khối u và chọn lọc trên khối u.
Capecitabine không phải là chất độc tế bào trên in vitro. Tuy nhiên, trên in vivo, thuốc được biến đổi liên tiếp thành chất gốc độc tế bào là 5-fluorouracil (5-FU), chất này sẽ được chuyển hoá tiếp.
Sự hình thành 5-FU tại khối u nhờ xúc tác một cách tối ưu của yếu tố tạo mạch liên quan tới khối u là thymidine phosphorylase (dThdPase), nhờ đó làm giảm tối đa mức độ của mô lành với 5-FU trong cơ thể.
Sự biến đổi sinh học tuần tự của men từ capecitabine thành 5-FU dẫn tới nồng độ của 5-FU cao hơn trong mô khối u. Sau khi cho bệnh nhân bị ung thư đại trực tràng (N=8) uống capecitabine, tỉ số nồng độ của 5FU ở khối u đại trực tràng so với các mô gần kề là 3,2 (dao động từ 0,9 đến 8,0). Tỉ số nồng độ ở khối u so với huyết tương là 21,4 (dao động từ 3,9 đến 59,9) trong khi tỉ số ở các mô khỏe mạnh so với huyết tương là 8,9 (dao động từ 3,0 đến 25,8). Hoạt tính của thymidine phosphorylase cao hơn gấp 4 lần ở khối u đại trực tràng so với mô bình thường bên cạnh.
Bệnh nhân ung thư vú, dạ dày, đại trực tràng, cổ tử cung, và buồng trứng có nồng độ thymidine phosphorylase cao hơn (có khả năng chuyển 5′-DFUR [5′-deoxy-5-fluorouridine] thành 5-FU) so với các mô bình thường tương ứng.
Các tế bào bình thường và các tế bào khối u chuyển hóa 5-FU thành 5-fluoro-2-deoxyuridine monophosphate (FdUMP) và 5-fluorouridine triphosphate (FUTP). Những chất chuyển hóa này sẽ làm tổn thương tế bào bằng hai cơ chế. Đầu tiên, FdUMP và đồng yếu tố folate N5-10-methylenetetrahydrofolate gắn với thymidylate synthase (TS) tạo nên một phức hợp gồm ba yếu tố đồng hoá trị.
Sự gắn kết này sẽ ức chế sự hình thành thymidylate từ uracil. Thymidylate là một tiền chất cần thiết của thymidine triphosphate, một chất cần thiết cho sự tổng hợp DNA, vì vậy sự thiếu hụt hợp chất này có thể ức chế sự phân chia tế bào. Thứ hai, các men sao chép nhân có thể kết hợp một cách nhầm lẫn FUTP thay vì uridine triphosphate (UTP) trong quá trình tổng hợp RNA. Lỗi chuyển hóa này có thể ảnh hưởng tới sự tổng hợp RNA và protein trong quá trình phát triển của tế bào ung thư.
Dược động học
Hấp thu
Sau khi uống, capecitabine được hấp thu nhanh chóng và rộng khắp, sau đó được chuyển hoá mạnh thành chất chuyển hóa 5′-deoxy-5-fluorocytidine (5′-DFCR) và 5’DFUR. Dùng cùng với thức ăn làm giảm tỉ lệ hấp thu capecitabine, nhưng chỉ ảnh hưởng rất ít.
Phân phối
Gắn kết với Protein. Các nghiên cứu huyết tương trên in-vitro đã chứng minh rằng tỉ lệ gắn kết protein của capecitabine, 5′-DFCR, 5′-DFUR và 5-FU lần lượt là 54%, 10%, 62% và 10%, chủ yếu gắn với albumin.
Chuyển hóa
Capecitabineđược chuyển hóa đầu tiên bởi men carboxylesterase ở gan thành 5′-DFCR, chất này sau đó được chuyển thành 5′-DFUR bởi cytidine deaminase, là men tập trung chủ yếu ở gan và mô khối u.
Sự hình thành 5-FU xảy ra chủ yếu tại vị trí khối u bởi yếu tố tạo mạch có liên quan đến khối u là dThdPase, do đó làm giảm tối đa mức độ của mô lành với 5-FU trong cơ thể. AUC huyết tương của 5-FU thấp hơn 6 đến 22 lần nồng độ sau khi truyền tĩnh mạch nhanh 5-FU (liều 600mg/m2). Các chất chuyển hóa của capecitabine chỉ trở nên có độc tính sau khi chuyển thành 5-FU và các chất đồng hóa của 5-FU (xem phần Cơ chế hoạt động).
5-FU được chuyển hóa tiếp thành các chất chuyển hóa không có hoạt tính dihydro-5-fluoruracil (FUH2), 5 fluoro-ureidopropionic acid (FUPA) và á-fluoro-â-alanine (FBAL) thông qua dihydropyrimidine dehydrogenase (DPD), chất này mang tính chuyển hóa chậm.
Đào thải
Thời gian bán thải (t1/2 tính bằng giờ) của capecitabine, 5′-DFCR, 5′-DFUR, 5 FU và FBAL tương ứng là 0.85, 1.11, 0.66, 0.76 và 3.23. Dược động học của capecitabine được đánh giá trên khoảng liều là 502-3514mg/m2/ngày. Các thông số của capecitabine, 5′-DFCR và 5′-DFUR được đo vào ngày đầu tiên và ngày 14 là như nhau. AUC của 5-FU là 30%-35% cao hơn vào ngày 14, nhưng không tăng lên sau đó (ngày 22). Tại liều điều trị, dược động học của capecitabine và các chất chuyển hoá của nó tỉ lệ với liều, trừ 5-FU.
Sau khi uống, các chất chuyển hóa của capecitabine được tìm thấy chủ yếu trong nước tiểu. 95.5% liều capecitabine được dùng tìm thấy trong nước tiểu. Bài tiết trong phân rất ít (2,6%). Chất chuyển hóa chính có trong nước tiểu là FBAL, chiếm 57% liều dùng. Khoảng 3% liều dùng được đào thải trong nước tiểu dưới dạng thuốc không đổi.
CHỈ ĐỊNH CỦA THUỐC XELODA
Ung thư vú
Xeloda được chỉ định phối hợp với docetaxel để điều trị những bệnh nhân ung thư vú tiến triển tại chỗ hoặc di căn sau khi thất bại với hóa trị liệu độc tế bào. Liệu pháp điều trị trước đây bao gồm anthracycline. Xeloda cũng được chỉ định như đơn trị liệu cho điều trị những bệnh nhân ung thư vú tiến triển tại chỗ hoặc di căn sau khi thất bại với chế độ hóa trị bao gồm anthracycline và taxane hoặc cho những ung thư khác mà không có chỉ định dùng anthracycline.
Ung thư đại trực tràng
Xeloda được chỉ định điều trị hỗ trợ cho những bệnh nhân ung thư đại tràng sau phẫu thuật.
Xeloda còn được dùng để điều trị cho những bệnh nhân ung thư đại trực tràng di căn.
Ung thư dạ dày
Xeloda phối hợp với hợp chất platin được chỉ định điều trị bước một cho những bệnh nhân ung thư dạ dày tiến triển.
CHỐNG CHỈ ĐỊNH
Xeloda được chống chỉ định trên những bệnh nhân được biết là quá mẫn với capecitabine hoặc với bất kỳ thành phần nào của thuốc.
Xeloda được chống chỉ định trên những bệnh nhân có tiền sử các phản ứng nghiêm trọng và không dự đoán trước với fluoropyrimidine hoặc được biết là quá mẫn với fluorouracil.
Cũng như các fluoropyrimidine, Xeloda được chống chỉ định trên những bệnh nhân được biết là có thiếu hụt DPD (dihydropyrimidine dehydrogenase).
Không nên dùng Xeloda cùng với sorivudine hoặc các chất tương tự có liên quan về mặt hóa học, như là brivudine (xem phần Tương tác thuốc).
Xeloda được chống chỉ định trên những bệnh nhân bị suy gan nặng (Child Pugh C)
Xeloda được chống chỉ định trên những bệnh nhân bị suy thận nặng (độ thanh thải creatinine giảm dưới 30 ml/phút).
Nếu có chống chỉ định của bất kỳ thuốc nào trong điều trị kết hợp, thì không dùng thuốc đó.
TÁC DỤNG KHÔNG MONG MUỐN
Tác dụng phụ Xeloda phổ biến có thể bao gồm:
đau dạ dày hoặc khó chịu, táo bón; cảm giác mệt mỏi; phát ban da nhẹ; hoặc là tê hoặc ngứa ran ở tay hoặc chân của bạn.
Gọi cho bác sĩ của bạn ngay lập tức nếu bạn có: dấu hiệu phản ứng dị ứng với Xeloda: nổi mề đay; khó thở; sưng mặt, môi, lưỡi hoặc cổ họng của bạn.
buồn nôn, chán ăn, ăn ít hơn bình thường, nôn (nhiều hơn một lần trong 24 giờ);
tiêu chảy nặng (hơn 4 lần mỗi ngày, hoặc vào ban đêm);
phồng rộp hoặc loét trong miệng, nướu đỏ hoặc sưng, khó nuốt;
đau, đỏ, sưng, phồng rộp hoặc bong tróc da ở tay hoặc chân của bạn;
triệu chứng mất nước – cảm thấy rất khát hoặc nóng, không thể đi tiểu, đổ mồ hôi nhiều, hoặc da nóng và khô;
vấn đề về tim: đau ngực hoặc áp lực, nhịp tim không đều, khó thở ngay cả khi gắng sức nhẹ, sưng hoặc tăng cân nhanh;
vấn đề về thận: ít hoặc không đi tiểu; đi tiểu đau hoặc khó khăn; sưng ở bàn chân hoặc mắt cá chân của bạn; cảm thấy mệt mỏi hoặc khó thở;
các vấn đề về gan: buồn nôn, đau dạ dày trên, ngứa, cảm giác mệt mỏi, chán ăn, nước tiểu sẫm màu, phân màu đất sét, vàng da;
số lượng tế bào máu thấp: sốt hoặc các triệu chứng cúm khác, ho, lở da, da nhợt nhạt, dễ bầm tím, chảy máu bất thường, cảm thấy nhẹ đầu, nhịp tim nhanh; hoặc là
phản ứng da nghiêm trọng: sốt, đau họng, sưng ở mặt hoặc lưỡi, nóng rát ở mắt, đau da, sau đó là phát ban da đỏ hoặc tím lan rộng đặc biệt là ở mặt hoặc trên cơ thể và gây phồng rộp và bong tróc.
HƯỚNG DẪN SỬ DỤNG
Liều dùng
Bệnh nhân ung thư đại trực tràng, ung thư vú 1250 mg/m2, 2 lần/ngày (sáng, tối) x 14 ngày, sau đó là 7 ngày nghỉ thuốc.
Bệnh nhân điều trị kết hợp: Ung thư vú khởi đầu 1250 mg/m2, 2 lần/ngày x 2 tuần, phối hợp docetaxel, sau đó lá 1 tuần nghỉ;
Ung thư dạ dày, ung thư đại trực tràng 800-1000 mg/m2/lần x 2 lần/ngày x 2 tuần, sau đó 7 ngày nghỉ thuốc hoặc 625 mg/m2/lần x 2 lần/ngày khi điều trị liên tục.
Cách dùng:
Nên dùng thuốc Xeloda cùng với thức ăn: Uống với nước trong vòng 30 phút sau ăn.Chống chỉ định: Tiền sử phản ứng nghiêm trọng & không dự đoán trước với fluoropyrimidine hoặc quá mẫn với fluorouracil. Thiếu hụt DPD. Suy gan/thận nặng.
TƯƠNG TÁC THUỐC
Hãy thông báo với bác sĩ nếu bạn đang sử dụng những thuốc sau:
thuốc điều trị bệnh gút (allopurinol),
thuốc làm loãng máu (coumarin, warfarin),
một số loại thuốc chống vi-rút (sorivudine và brivudine),
thuốc trị co giật hoặc run (phenytoin),
interferon alpha,
xạ trị và một số loại thuốc dùng để điều trị ung thư (axit folinic, oxaliplatin, bevacizumab, cisplatin, irinotecan),
thuốc dùng để điều trị thiếu axit folic.
MUA THUỐC XELODA Ở ĐÂU? GIÁ BAO NHIÊU?
Thuốc Xeloda là thuốc gì? Thuốc Xeloda mua ở đâu chính hãng? Giá thuốc Xeloda bao nhiêu? Công dụng thuốc Xeloda là gì? Thuốc Xeloda có tốt không? Thuốc Xeloda trên đây là các câu hỏi mà bạn đọc hay gặp phải, để được tư vấn về giá, địa chỉ mua thuốc Xeloda chính hãng giá rẻ nhât xin LH Ds Dũng 0978.342.324 để được tư vấn.Thuốc Xeloda có bán tại hệ thống thuockedon24h.com, với giá rẻ nhất giao hàng toàn quốc.








Reviews
There are no reviews yet.